手順
- 排液する。
- 氷酢酸を0.2mlほど加える。
- 酸性フクシン染色液を1〜2滴投入。
- 容器に蓋をし常温でしばらく置く 実体顕微鏡下でときどき観察 適度に染まるまで(5分から8時間ぐらい?)。
- 排液して氷酢酸を0.2mlほど加える
- ほとんど染まらないか、ランダムにまだらに染まる場合は 脱ロウが不十分と思われるので脱ロウからやり直す。
- 氷酢酸と酸性フクシン染色液の混合液が透明に近くなったら染色液を追加する。
- 濃くなりすぎた場合やムラができた場合は、 70%エタノールにつけてしばらく置いておく。
▼動画は2倍速
染色の進行
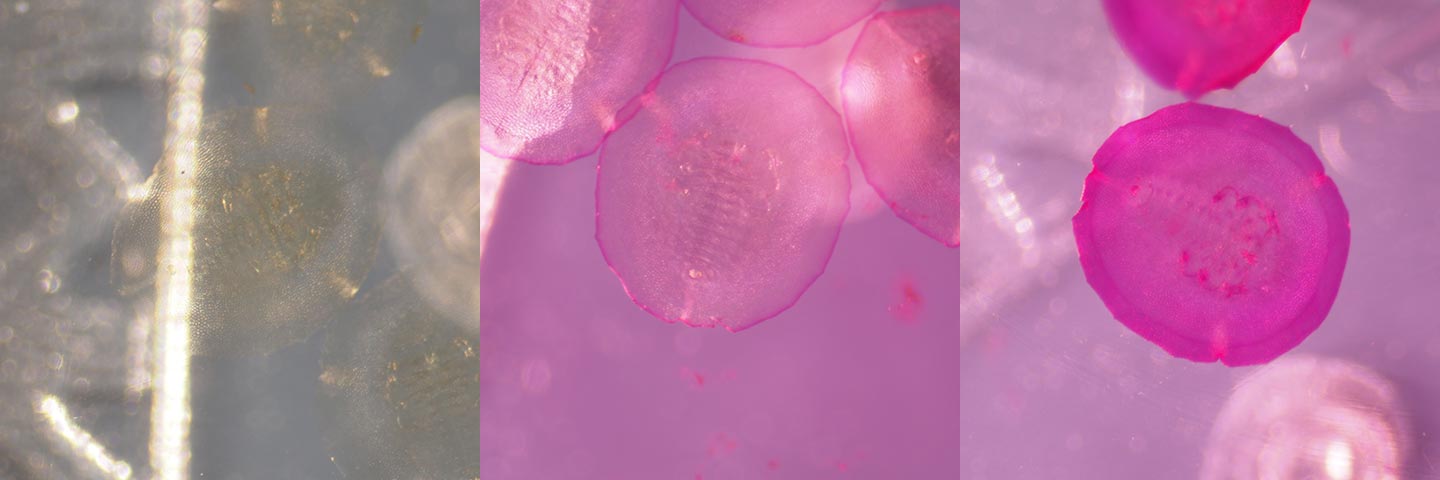
酸性フクシン染色液
酸性フクシンは黒っぽい粉末。 あらかじめ染色液にしてスポイト瓶に保存しておく。 染色液の作り方はHenderson2011によると 酸性フクシン0.35g, 蒸留水75ml(精製水で良いと思う), 氷酢酸25mlだが、 このままだと濃すぎると思う。 私はこれをさらに20倍ぐらいに薄めて使用している。